Radioisótopos
Todos los átomos cuyos núcleos tienen el mismo número de protones constituyen un elemento químico. Como tienen el mismo número de protones, tienen el mismo número de electrones y, por consiguiente, las mismas propiedades químicas. Cuando su número de neutrones es diferente, reciben la denominación de "isótopos". Cada isótopo de un elemento determinado se designa por el número total de sus nucleones (protones y neutrones).
Por ejemplo, el uranio 238 y el uranio 235 tienen ambos 92 electrones. Su núcleo tiene 92 protones. El isótopo 238 tiene 146 neutrones, o sea, 3 neutrones más que el uranio 235.
Los radioisótopos son aquellos isótopos que son radiactivos.
Usos de los radioisótopos
Como se expondrá en el trabajo, existe gran cantidad de usos que se da a la radiación, por ello, sólo mencionaré los principales usos de algunos radioisótopos
Los radioisótopos son ampliamente usados en:
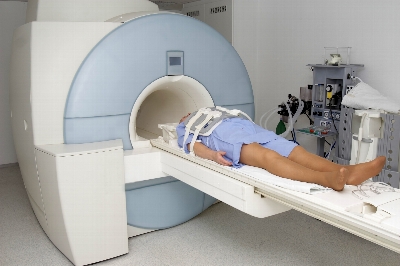 Medicina nuclear. Permitiendo a los médicos explorar estructuras corporales y funciones in vivo (o sea en cuerpos vivos) con una invasión mínima del paciente. También se usan en radioterapia para tratar algunos tipo de cáncer y otras condiciones medicas que requieren la destrucción de células malignas.
Medicina nuclear. Permitiendo a los médicos explorar estructuras corporales y funciones in vivo (o sea en cuerpos vivos) con una invasión mínima del paciente. También se usan en radioterapia para tratar algunos tipo de cáncer y otras condiciones medicas que requieren la destrucción de células malignas. En ingeniería y o industria se usan como trazadores industriales, radiografiado de soldaduras, especialmente en recipientes de alta presión, curado de plásticos, preservación de alimentos, y fuente de energía para generadores de electricidad.
En ingeniería y o industria se usan como trazadores industriales, radiografiado de soldaduras, especialmente en recipientes de alta presión, curado de plásticos, preservación de alimentos, y fuente de energía para generadores de electricidad.En agronomía se usan fertilizantes "rotulados" con un isotopo particular, tal como Nitrógeno-15 y Fosforo-32. Permitiendo determinar cuánto absorbe la planta y cuanto se pierde.
La vida media de ciertos isotopos permite estimar la antigüedad de las rocas, de los hallazgos arqueológicos y hasta de una botella de vino.
 El carbono-14 (C-14) se utiliza para determinar la edad de los fósiles o de restos arqueológicos que contengan material orgánico.
El carbono-14 (C-14) se utiliza para determinar la edad de los fósiles o de restos arqueológicos que contengan material orgánico. El potasio-40(K-40) se utiliza para fechar cuerpos muy antiguos, como las rocas de la corteza terrestre y lunar. Midiendo la cantidad de potasio-4 en las rocas se puede determinar su edad.
El potasio-40(K-40) se utiliza para fechar cuerpos muy antiguos, como las rocas de la corteza terrestre y lunar. Midiendo la cantidad de potasio-4 en las rocas se puede determinar su edad.El tritio (H-3) es un isotopo del hidrogeno y tiene una vida media de 12,3 años, por ello se utiliza para fechar objetos hasta 100 años de antigüedad, como los vinos añejos.



No hay comentarios:
Publicar un comentario